重症嗜酸性粒细胞型哮喘
2016/10/26
沈阳军区总医院呼吸与重症医学科 110016
哮喘是一种异质性疾病,通常以慢性气道炎症为特征。呼吸道症状如喘息、气短、胸闷和咳嗽,随时间而强度变化,伴随不同程度的呼气性气流受限。慢性气道炎症包括:1.多种炎症细胞参与,如肥大细胞、嗜酸性粒细胞、嗜中性粒细胞、Th2淋巴细胞等;2.多种炎症介质参与,如IL-5、IL-13、IL-4等;3.作用于多种结构细胞,如气道上皮细胞、气道平滑肌细胞、血管内皮细胞等。
2014年美国胸科学会/欧洲呼吸学会(ERS/ATS)对重症哮喘的定义是:哮喘患者(>6岁)的哮喘诊断正确、合并症已排除或得到妥善处理,前一年需要高剂量ICS联合另一种控制药和/或全身性激素治疗(GINA 4–5级治疗)才能控制或仍未控制的哮喘,在使用大剂量吸入糖皮质激素或全身激素(或联合生物制剂) 减量时发生恶化[1]。重症哮喘的表型主要包括早发型过敏性重症哮喘、晚发型嗜酸性粒细胞性重症哮喘、中性粒细胞型重症哮喘、肥胖型重症哮喘,如图1[2]。其中,晚发型嗜酸性粒细胞性重症哮喘由于患者比例相对较高、高剂量激素疗效差且新型疗法可能带来机遇引起了人们的广泛关注。
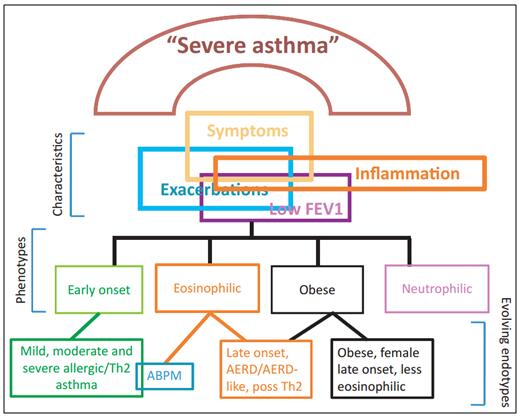
一 、晚发型嗜酸性粒细胞性重症哮喘及其特点
晚发型嗜酸性粒细胞性重症哮喘一般起病年龄大于12岁(有争议),同时达到重症哮喘标准,尽管高剂量的吸入或全身使用糖皮质激素,支气管活检和诱导痰中嗜酸性粒细胞仍持续升高。该分型是基于诱导痰的炎症亚型中的一种,指诱导痰中嗜酸性粒细胞比例≥2%(有争议)[3] 我国为2.3%。
其主要特点包括,1.50%-67%的重症哮喘患者,大气道有持续的嗜酸性粒细胞增高;2.症状更多,FEV1更低,更易出现重度加重,治疗困难;3.更易患鼻窦疾病、累及外周气道和出现气道重构、固定的气道梗阻;4.持续性气道嗜酸粒细胞性炎症可能由不同的信号通路参与,与PGD2/CRTH2通路有更大的关联性;5.2型先天性淋巴免疫细胞(Type-2 innate lymphoid cells, ILC2)参与炎症过程;6.血小板炎性细胞之间的相互影响及LTE4生成增多;7.部分糖皮质激素治疗无效;8.部分缺乏过敏性特征(低IgE);9.普遍存在鼻息肉及对阿司匹林敏感;10.极高的死亡率,难以治疗;11.新型疗法可能带来机遇[4]。
二、 晚发型嗜酸性粒细胞性重症哮喘可能的分子机制
哮喘的发病机制尚不完全清楚。免疫-炎症反应是形成哮喘的病理基础。经典的发病模式是以 CD4+Th2 细胞为主。约 50% 的哮喘患者,持续气道嗜酸性粒细胞增多,表现为气道内以嗜酸性粒细胞浸润为主的变态反应性炎症。哮喘气道内嗜酸粒细胞性炎症主要由两条通路引发。过敏性嗜酸粒细胞性哮喘中,树突状细胞把过敏原传递给CD4+T细胞(包括Th2细胞),由此产生IL-4、IL-5、IL-13等炎症介质,并导致B细胞内IgE的转化,气道内嗜酸粒细胞浸润及粘液分泌过多。非过敏性嗜酸粒细胞性哮喘中,空气污染物、细菌及脂糖类物质诱导气道上皮细胞因子的释放,包括IL-33、IL-25和TLSP,由此分别通过刺激不同的受体(IL-17RB、ST2、TLSPR)这种不依赖变应原的方式激活ILC2S,激活ILC2s产生大量的IL-5和IL-13,导致嗜酸粒细胞浸润、气道粘液分泌增多和气道高反应性[5]。在成人晚发型嗜酸性粒细胞增多的重症哮喘患者中,使用激素治疗后效果不佳, 提示对激素反应不敏感, 但使用抗 IL-5单克隆抗体(mepolizumab)后有效,可能与嗜酸粒细胞凋亡功能缺陷,以及大量炎性介质干扰激素抗炎作用有关[6]。
三、 晚发型嗜酸性粒细胞性重症哮喘临床相关生物标记物
1.嗜酸性粒细胞:气道内嗜酸性粒细胞炎症水平与哮喘病情的轻中重密切相关,是活动性变应性炎症的生物标志物。1990年Jean等学者研究表明,哮喘患者外周血嗜酸性粒细胞明显增高,同时肺泡灌洗液内嗜酸性粒细胞及其阳离子蛋白亦明显增高,并且均与疾病的严重程度、肺功能明显呈正相关[7,8]。
2.呼出气一氧化氮(fractional exhaled nitric oxide,FeNO):与气道嗜酸性粒细胞计数正相关,与气道高反应相关,能很好的评估气道炎症。FeNO作为间接反应气道炎症水平的指标,具有非侵袭性、可重复、安全、可定量等优点。NO是气道上皮细胞在一氧化氮合酶(iNOS)作用下产生的,NO释放量的多少和嗜酸粒细胞性炎症程度相关。Th2炎症伴随呼出气NO的增高,NO是Th2细胞介导的嗜酸性炎症标记物。Th2炎症的IL-4/IL-13为局部通路,可以被ICS所阻断,IL-5的通路需要用口服激素来阻断。该指标有助临床上哮喘的诊断和监测。有胸闷、气短等症状的成年患者若FeNO值大于50ppb(parts per billion),则高度怀疑哮喘可能,并且该值预示着对于激素治疗的敏感性。若FeNO小于25ppb,则预示着嗜酸性粒细胞性哮喘的可能性极低,并且激素治疗很可能无效[9]。监测FeNO值的变化可了解哮喘的控制水平,若FeNO值持续增高,则表明患者可能长期暴露于过敏源之中,或者吸入药物应用的不理想、不规范,或者依从性差等[10]。然而,FeNO亦有局限性,FeNO正常值上限因人而异,目前很难用统一的标准界定;FeNO值易受测量技术、呼出气流速及鼻部NO污染物等因素的影响;此外,FeNO还受年龄(尤其儿童)、变应性、性别、体重和身高的影响[11]。
M. Berry等学者研究表明,经吸入性糖皮质激素治疗后的难治性哮喘患者肺泡灌洗液一氧化氮含量高于轻中度哮喘患者,表明与轻中度哮喘患者相比,吸入性糖皮质激素对难治性哮喘气道炎症改善状况不理想。使用双倍剂量吸入性皮质醇类药物的难治性哮喘患者吸药前后肺泡灌洗液一氧化氮浓度变化不明显,而口服皮质醇类药物的难治性哮喘患者服药前后肺泡灌洗液一氧化氮浓度明显降低,表明难治性哮喘的气道炎症对于口服激素较吸入激素更敏感、有效[12]。
3.溴酪氨酸(Bromotyrosine,BrTyr) :是嗜酸性粒细胞活化的可靠生化指标;可以在血液和尿中高度稳定存在并被检测到;可以预测成人和儿童的急性加重。2011年Samuel H等学者研究发现,尿液中溴酪氨酸水平明显与哮喘控制程度(哮喘控制量表评分)呈负相关:溴酪氨酸基线值高的患者,在未来6周内,哮喘未完全控制的发生率高出18.1倍(95% CI 2.1–153.1, P = .0004)、哮喘急性加重的发生率高出4倍(95% CI 1.1–14.7, P = .03)[13]。
然而,以上单一指标不能很好的评估病情和预测哮喘对治疗的反应,均有其局限性, 如图2联合应用更准确[14]。

四、 晚发型嗜酸性粒细胞性重症哮喘临床治疗及进展
1.传统药物治疗: 通常采取GINA推荐4-5级药物治疗方案,即成人吸入氟替卡松量>500 μg/d(或其等价剂量),联合吸入长效β2受体激动剂等两种或两种以上缓解药物(如白三烯受体拮抗剂、抗胆碱能药物、茶碱等)。然而,采用规范长期治疗,同时去除诱发因素,合理控制并存疾病后,仍不能达到理想控制目标的患者,应考虑采取进一步治疗措施。
2.生物制剂治疗:这种治疗方式旨在通过抑制 Th2介导的炎症反应环节中的某些细胞因子或趋化因子,发挥抗炎作用。表 1 总结了目前正在临床研究的靶向制剂。
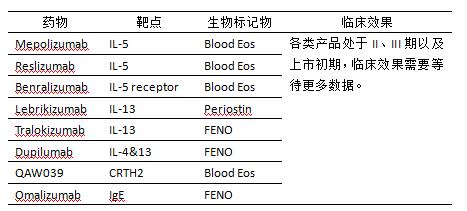
抗IgE单克隆抗体: Omalizumab是自2006年起GINA 推荐作为治疗重症哮喘的靶向药物之一。通过阻断游离的IgE与其效应细胞(肥大细胞、嗜碱性粒细胞)表面受体结合,但不会诱导相应效应细胞的脱颗粒反应,可以显著地改善哮喘急性发作症状,减少糖皮质激素使用量,减少哮喘急性加重和住院率。研究发现,在特应性、早发性、Th2细胞介导的重症哮喘患者中,气道中肥大细胞、嗜碱性粒细胞表面IgE 受体高表达。当血清总IgE水平在30-700 IU/ml时,抗IgE单抗(omalizumab)能降低血清游离IgE水平, 调节周围血嗜碱细胞的IgE受体,显著降低鼻部和支气管的嗜酸细胞、肥大细胞及T细胞和B细胞的数目,有效减少严重过敏性哮喘急性发作次数。2014年ERS/ATS对于重症哮喘治疗指南中推荐,变应性重症哮喘患者血清总IgE水平在30-700 IU/ml时可考虑试验性使用抗IgE单抗。但由于目前该药物价格较高,限制了其广泛应用[15]。
抗IL- 5单克隆抗体: IL- 5是由Th2细胞分泌的细胞因子,参与调控嗜酸性粒细胞的分化、成熟、黏附、浸润、凋亡,并能够为嗜酸性粒细胞从骨髓迁移至肺部及其他器官提供重要的信号。Mepolizumab 是一种实验性全人源化单克隆抗体,特异性靶向结合IL- 5。其作用机制是: 阻断 IL- 5与嗜酸性粒细胞表面受体的结合,抑制IL- 5对受体的结合作用,降低血液、组织、痰液中的嗜酸性粒细胞水平,从而降低嗜酸性粒细胞所介导的炎症。近期的两项Ⅱ期临床试验观察结果显示,IL- 5单克隆抗体可明显减少难治性嗜酸性粒细胞增多性哮喘患者的恶化频率。通过抑制IL- 5可以阻止嗜酸性粒细胞成熟、分化及迁移到肺组织从而治疗哮喘[16-20]。
其他新型生物制剂,都是针对晚发型嗜酸性粒细胞性重症哮喘炎症反应机制,抑制相应的细胞因子释放,阻断炎症反应发生,达到有效减少哮喘急性发作。
3.小颗粒状吸入性糖皮质激素:2015年David Hodgson等学者将难治性哮喘患者(30例)随机分成两组:环索奈德(Ciclesonide)组和安慰剂组,每组15人。分别对两组患者进行痰嗜酸粒细胞比率进行测量(23VS9.6),然后两组分别进行2周的高剂量吸入性糖皮质激素治疗并随机抽取部分患者(10例VS11例)测得其痰嗜酸粒细胞比率0%(即哮喘病情得到控制后)再分别以环索奈德及安慰剂进行8周治疗后取患者痰液(11例VS13例)测量痰嗜酸粒细胞比率(2.3%VS4.5%)并分别对两组进行组内比较,结果表明环索奈德组无明显统计学差异,安慰剂组有统计学差异。该研究表明,小颗粒吸入性糖皮质激素能够有效控制嗜酸粒细胞性持续性难治性哮喘。患者持续进展的嗜酸性粒细胞炎症并非真得“难治”,合适的吸入方式、剂量或许能得到令人满意的效果[21]。
4.阿司匹林诱发哮喘:占成人哮喘发作的20%,占成人重症嗜酸性粒细胞型哮喘的40%,应当得到重视。特点:1.有明确的用药史;2.常伴有鼻窦炎和鼻息肉,常先于哮喘发病;3.是局部及全身对阿司匹林以及其他COX-1抑制剂的过敏反应;4.气道炎症通常对局部激素反应不佳,系统性治疗更为有效[4]。通常,患者尿液、支气管肺泡灌洗液中的白三烯的含量明显增高。阿司匹林诱发哮喘总的治疗原则:对于急性病例,首先停用阿司匹林,同时给予吸氧、保持呼吸道通畅、吸痰等处理,并酌情给予抗组胺药、β受体激动剂、糖皮质激素等药物,对重症哮喘应及早进行机械辅助通气;对于慢性病例,可口服或吸入糖皮质激素。若合用抗组胺药和肥大细胞稳定剂色甘酸、酮替芬可减轻症状、减少糖皮质激素用量。白三烯受体拮抗药和5-脂氧合酶抑制药也有一定疗效。对于无法避免使用阿司匹林和其他非甾体类消炎药的患者,可进行阿司匹林脱敏治疗。
参考文献:
1. Chung KF, Wenzel SE, Brozek JL, et al. International ERS/ATS guidelines on definition, evaluation and treatment of severe asthma. Eur Respir J, 2014, 43(2):343-373.
2.Wenzel S. Severe asthma: from characteristics to phenotypes to endotypes. Clin Exp Allergy, 2012, 42(5):650-8.
3.Gibson PG, McDonald VM, Marks GB, et al. Asthma in older adults. Lancet, 2010, 376(9743): 803-13.
4.Chung KF, Adcock IM. Clinical phenotypes of asthma should link up with disease mechanisms. Curr Opin Allergy Clin Immunol, 2015, 15(1):56-62.
5. Porsbjerg CM, Gibson PG, Pretto JJ, et al. Relationship between airway pathophysiology and airway inflammation in older asthmatics. Respirology, 2013, 18(7): 1128-1134.
6. Pavord ID, Korn S, Howarth P, et al. Mepolizumab for severe eosinophilic asthma(DREAM): a multicentre, double-blind, placebo-controlled trial. Lancet, 2012, 380(9842): 651-659.
7. Bousquet J, Chanez P, Lacoste JY ,et al. Eosinophilic inflammation in asthma. N Engl J Med, 1990, 323(15):1033-9.
8. Katz LE, Gleich GJ, Hartley BF, et al. Blood eosinophil count is useful biomarker to identify
patients with severe eosinophilic asthma. Ann Am Thorac Soc, 2014, 11(4):531-6.
9. Chrystalla Loutsios, Neda Farahi, Linsey Porter, et al. Biomarkers of eosinophilic inflammation in asthma. Expert Rev Respir Med, 2014 Apr;8(2):143-50.
10. McNicholl DM, Stevenson M, McGarvey LP, et al. The utility of fractional exhaled nitric oxide suppression in the identification of nonadherence in difficult asthma. Am J Respir Crit Care Med, 2012, 186(11):1102-8.
11. Dweik RA, Boggs PB, Erzurum SC, et al. An official ATS clinical practice guideline: interpretation of exhaled nitric oxide levels(FENO) for clinical applications. Am J Respir Crit Care Med, 2011, 184:602-15.
12. Berry M, Hargadon B, Morgan A, et al. Alveolar nitric oxide in adults with asthma:evidence of distal lung inflammation in refractory asthma. Eur Respir J, 2005, 25: 986–991.
13. Wedes SH, Wu W, Comhair SA et al. Urinary Bromotyrosine Measures Asthma Control and Predicts Asthma Exacerbations in Children. J Pediatr, 2011,159(2): 248–55.
14. Wedes SH, Khatri SB, Zhang R, et al. Noninvasive markers of airway inflammation in asthma. Clin Transl Sci, 2009, 2(2):112-7.
15. Li J, Kang J, Wang C, et al. Omalizumab Improves Quality of Life and Asthma Control in Chinese Patients With Moderate to Severe Asthma: A Randomized Phase III Study. Allergy Asthma Immunol Res, 2016 , 8(4):319-28.
16.Powell C, Milan SJ, Dwan K, et al. Mepolizumab versus placebo for asthma. Cochrane Database Syst Rev, 2015, 7:CD010834.
17. Bel EH, Wenzel SE, Thompson PJ, et al.Oral glucocorticoid-sparing effect of mepolizumab in
eosinophilic asthma. N Engl J Med, 2014, 371(13):1189-97.
18.Fainardi V, Pisi G, Chetta A, et al. Mepolizumab in the treatment of severe eosinophilic asthma. Immunotherapy, 2016, 8(1):27-34.
19.Patterson MF, Borish L, Kennedy JL, et al. The past, present, and future of monoclonal antibodies to IL-5 and eosinophilic asthma: a review. J Asthma Allergy, 2015, 8:125-34.
20. Varricchi G, Bagnasco D, Borriello F, et al.Interleukin-5 pathway inhibition in the treatment of eosinophilic respiratory disorders: vidence and unmet needs. Curr Opin Allergy Clin Immunol, 2016, 16(2):186-200.
21. Hodgson D, Anderson J, Reynolds C, et al. A randomised controlled trial of small particle inhaled steroids in refractory eosinophilic asthma (SPIRA). Thorax, 2015, 70:559-565.
上一篇:
固有免疫在哮喘发病中的作用
下一篇:
肥胖型哮喘发病机制









